Enriquecimiento del uranio

El enriquecimiento del uranio es un proceso necesario para crear un combustible nuclear eficaz a partir del uranio extraído, aumentando el porcentaje de uranio-235 que se somete a la fisión con neutrones térmicos. Aunque muchos reactores requieren combustible de uranio enriquecido, el CANDU de diseño canadiense, el reactor Magnox británico y el reactor de sales fundidas propuesto pueden utilizar uranio natural como combustible.[2]
El combustible nuclear se extrae de los yacimientos naturales de mineral de uranio y luego se aísla mediante reacciones químicas y procesos de separación. Estos procesos químicos utilizados para separar el uranio del mineral no deben confundirse con los procesos físicos y químicos utilizados para enriquecer el uranio. En su forma aislada, el uranio se conoce como torta amarilla ("yellowcake" en inglés) y tiene la fórmula química U3O8. Sin embargo, el uranio natural no tiene una concentración suficientemente alta de 235U, con sólo un 0.72% aproximadamente, siendo el resto 238U.[3] Debido a que el uranio-238 es fisionable y no fisible, es necesario aumentar la concentración de uranio-235 antes de poder utilizarlo eficazmente como combustible nuclear. El objetivo del enriquecimiento del uranio es aumentar el porcentaje del isótopo uranio-235 con respecto a los demás isótopos, con un porcentaje necesario de alrededor del 4% para los reactores de agua ligera.[3]
Procesos de enriquecimiento
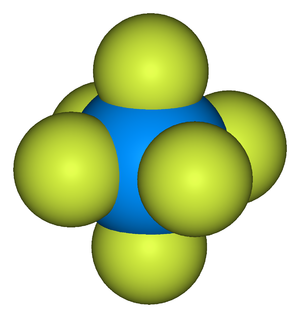
El enriquecimiento requiere que el uranio esté en forma gaseosa, y la forma más sencilla de conseguirlo es convertirlo en una sustancia química diferente conocida como hexafluoruro de uranio. El uranio necesita estar en forma gaseosa para el enriquecimiento debido a las diferentes propiedades químicas y físicas que tienen los distintos isótopos (U-235 y U-238). Estas diferencias se aprovechan y manipulan más fácilmente cuando el uranio está en forma gaseosa.
El proceso de transformación del concentrado de óxido de uranio a hexafluoruro de uranio se realiza en una planta de conversión, que es el primer paso para el uranio después de salir de una mina. El principal proceso de conversión utilizado en Canadá, Francia y Rusia se conoce como "proceso húmedo" e implica múltiples etapas de conversión química. En primer lugar, el concentrado de óxido de uranio se disuelve en ácido nítrico (HNO3), lo que genera nitrato de uranilo (UO2(NO3)2). Este nitrato de uranilo se purifica, se evapora y, finalmente, se descompone térmicamente para formar polvo de trióxido de uranio (UO3). Después hay dos procesos de horno en los que el UO3 se convierte en UO2, y luego se hace reaccionar con fluoruro de hidrógeno (HF), para producir tetrafluoruro de uranio (UF4). Por último, el UF4 se introduce en un reactor de lecho fluidizado y se hace reaccionar con flúor gaseoso para producir UF6. Tras el proceso de conversión, el UF6 necesita ser refinado aún más debido a la presencia de impurezas.[4]
Difusión gaseosa
Durante muchos años, el proceso principal fue la difusión gaseosa. Para separar físicamente el uranio, el uranio de torta amarilla se transformaba primero químicamente en hexafluoruro de uranio (UF6). Este producto químico se encuentra en su forma sólida en condiciones normales, pero se transforma en gas si se eleva mínimamente la temperatura o se reduce la presión.[3] Como las moléculas de 235UF6 son un poco más livianas que las de 238UF6, se mueven más rápidamente como gas por difusión. Por lo tanto, si el hexafluoruro de uranio se hace pasar por una tubería muy larga, el gas que emerge en el extremo de la tubería tendrá un porcentaje un poco mayor de 235U. Sin embargo, la tubería debe ser extremadamente larga, ya que el 235UF6, más liviano, se somete a la difusión sólo un 0.43% más rápido que el 238UF6.[3] Debido a esto, el método de difusión gaseosa ya no se utiliza ampliamente.
Centrifugadoras de gas

En la actualidad, el enriquecimiento se consigue mediante una centrifugadora especial llamada centrifugadora de gases. El proceso de separación se basa en la diferencia de masa de las moléculas (véase la difusión gaseosa más arriba). Aquí, el hexafluoruro de uranio se introduce en un cilindro evacuado que contiene un rotor. Cuando estos rotores giran a gran velocidad, el 238UF6, más pesado, se acumula cerca de las paredes del cilindro, mientras que el 235UF6, un poco más liviano, se acumula cerca del eje central. A continuación se extrae el producto enriquecido. Este método es preferible a la difusión gaseosa, ya que sólo requiere un 3% de la energía para separar el uranio.[3] Un método de separación centrífuga es mucho más eficiente energéticamente que la difusión, ya que sólo requiere unos 50-60 kWh por SWU (unidad de trabajo de separación, que es la cantidad de separación realizada por un proceso de enriquecimiento).[2] Además, estas plantas pueden ser más pequeñas, ya que no requieren una tubería extremadamente larga. Para que la separación sea eficaz, estas centrifugadoras deben girar rápidamente, generalmente a 50 000-70 000 rpm.[6]
Aunque las centrifugadoras contienen menos uranio que una etapa de difusión, son capaces de separar los isótopos de forma mucho más eficiente. Las etapas de centrifugación suelen estar compuestas por un gran número de centrifugadoras en paralelo, formando una cascada.
Separación de isótopos por láser
El uso de láseres en un proceso de separación está aún en desarrollo. Esta técnica de separación requiere un menor aporte de energía y otras ventajas económicas. En este proceso, un láser con una frecuencia muy específica interactúa con un gas o vapor. Como la frecuencia tiene una energía asociada, la interacción del rayo con el gas permite la excitación o ionización de determinados isótopos del vapor. Con esta excitación, puede ser posible separar las moléculas que contienen un isótopo específico para recoger sólo el isótopo excitado.[6]
Problemas medioambientales
En la mayoría de los procesos de enriquecimiento sólo están involucrados materiales radiactivos naturales de larga vida. El uranio es poco radiactivo, pero su toxicidad química es mucho más importante. Por ello, las medidas de protección necesarias para una planta de enriquecimiento son similares a las de otras industrias químicas. Cuando se expone a la humedad, el hexafluoruro de uranio forma un ácido muy corrosivo, el ácido fluorhídrico. Cualquier fuga de este producto químico es indeseable y, para evitarlo, casi todas las áreas de una planta de enriquecimiento mantienen el gas de hexafluoruro de uranio por debajo de la presión atmosférica,[2] lo que impide cualquier fuga hacia el exterior. Además, en las zonas en las que se requieren presiones más elevadas, se aplica una doble contención y se recogen y tratan los gases de escape.
El enriquecimiento representa aproximadamente la mitad del coste del combustible nuclear en un reactor de agua ligera (un BWR o PWR) y el 5% del coste de la electricidad generada. Anteriormente, el enriquecimiento ha sido la principal fuente de gases de efecto invernadero del ciclo del combustible nuclear, ya que la electricidad utilizada para el enriquecimiento se generaba con carbón. Aunque hay emisiones de gases de efecto invernadero asociadas, es sólo un 0.1% de las emisiones de una central eléctrica de carbón equivalente.[2]
Referencias
- ↑ Wikimedia Commons. (May 5, 2016). Uraninite [Online]. Available: https://commons.wikimedia.org/wiki/File:Uraninite-usa32abg.jpg
- ↑ 2,0 2,1 2,2 2,3 World Nuclear Association. (June 17, 2015). Uranium Enrichment [Online]. Available: http://www.world-nuclear.org/info/Nuclear-Fuel-Cycle/Conversion-Enrichment-and-Fabrication/Uranium-Enrichment/
- ↑ 3,0 3,1 3,2 3,3 3,4 Jeff C. Bryan. (June 17, 2015). Introduction to Nuclear Science, 1st ed. Boca Raton, FL, U.S.A: CRC Press, 2009.
- ↑ World Nuclear Association. (May 12, 2016). Conversion and Deconversion[Online]. Available: http://www.world-nuclear.org/information-library/nuclear-fuel-cycle/conversion-enrichment-and-fabrication/conversion-and-deconversion.aspx
- ↑ Wikimedia Commons. (June 17, 2015). Gas Centrifuge Cascade [Online]. Available: https://commons.wikimedia.org/wiki/File:Gas_centrifuge_cascade.jpg#/media/File:Gas_centrifuge_cascade.jpg
- ↑ 6,0 6,1 Ian Hore-Lacy. (June 17, 2015). Nuclear Energy in the 12st Century, 1st Ed. Burlington, MA, U.S.A: Elsevier Inc, 2006.

