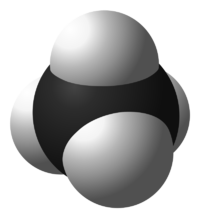
Metano
El metano es un alcano con la fórmula química CH4. Como hidrocarburo, puede sufrir una combustión de hidrocarburos que desprende calor. El metano es el principal componente hidrocarburo del gas natural, que es un tipo de combustible fósil.[2]
A las temperaturas y presiones habituales, es un gas y constituye alrededor del 95% del contenido del gas natural licuado, y alrededor del 80-90% del gas natural.[3] El metano es también un gas de efecto invernadero, como el dióxido de carbono (CO2). Su vida atmosférica es más corta que la del CO2, con 12 años,[4] pero esto se ve "compensado" por el hecho de que es más eficaz para atrapar el calor que el CO2, ya que el metano tiene un PCG (potencial de calentamiento global, también conocido como GWP) de 21.[5]
La combustión de metano (véase la simulación en la parte inferior de la página) proporciona una fracción significativa de la energía primaria del mundo, y se utiliza para la calefacción de los hogares, la cocción de alimentos, el calentamiento del agua y la generación de electricidad. Incluso puede proporcionar energía para el transporte. Sin embargo, esto significa que también contribuye significativamente al cambio climático, ya que este metano produce una buena cantidad del dióxido de carbono que los humanos emiten a la atmósfera.
Propiedades
A continuación se muestra una tabla con algunas de las propiedades básicas del metano.
| Fórmula química | CH4 |
| Masa molar | 16,04 gramos/mol |
| Densidad energética[6] | 55,5 MJ/kg |
| Punto de fusión | -183oC[7] |
| Punto de ebullición | -164oC[7] |
| PCG | 21 |
| Tiempo de vida atmosférico | 12 años |
Animación de la combustión
El metano libera su energía química mediante la combustión de hidrocarburos. A continuación se muestra una animación de la combustión de hidrocarburos que muestra la reacción neta que se produce cuando el metano se combina con el oxígeno.
La reacción de combustión de hidrocarburos libera energía térmica y es un ejemplo de reacción exotérmica. La reacción también tiene un valor de cambio de entalpía (ΔH) negativo.
Ver lecturas adicionales
- Energía química
- Enlace químico
- Combustión
- Energía primaria
- Tecnología de conversión de energía
- O explore una página al azar
Referencias
- ↑ (2014, Dec. 12). Methane-3D-space-filling [Online]. Available: http://commons.wikimedia.org/wiki/File:Methane-3D-space-filling.svg#mediaviewer/File:Methane-3D-space-filling.svg
- ↑ “NATURAL GAS FAQs,” Pacific Northern Gas RSS. [Online]. Available: http://www.png.ca/natural-gas-faqs/. [Accessed: 24-May-2017]
- ↑ (2014, Jun. 10). Composition of Natural Gas and LNG [Online]. Available: http://www.beg.utexas.edu/energyecon/lng/LNG_introduction_07.php
- ↑ (2014, Jun. 10). Direct Global Warming Potentials [Online]. Available: http://www.ipcc.ch/publications_and_data/ar4/wg1/en/ch2s2-10-2.html
- ↑ Direct Global Warming Potentials [Online]. Available: http://www.ipcc.ch/publications_and_data/ar4/wg1/en/ch2s2-10-2.html [Accessed: 24-May-2017.
- ↑ (2014, Dec. 12). Chemical Potential Energy [Online]. Available: http://physics.info/energy-chemical/
- ↑ 7,0 7,1 (2015, Jan. 29). Boiling Points And Structures Of Hydrocarbons [Online]. Available: http://www.elmhurst.edu/~chm/vchembook/501hcboilingpts.html