Demi-vie
La demi-vie est le temps nécessaire pour que la moitié de la valeur initiale d'une certaine quantité d'un élément radioactif se désintègre. Cela implique également qu'une demi-vie est le temps qu'il faut pour que l'activité d'une source se réduise à la moitié de sa valeur initiale.[2] Ces atomes radioactifs libèrent de l'énergie pour devenir de nouveaux types d'atomes à un rythme mesurable appelé désintégration radioactive.
Toutes les matières radioactives contiennent des noyaux instables, c'est-à-dire des noyaux qui vont se désintégrer. Certains noyaux d'une substance peuvent déjà être dans leur état stable, mais la proportion de noyaux stables et instables dans un échantillon peut varier. Les noyaux stables d'un échantillon sont immuables (et dans un état énergétique stable), mais les noyaux instables vont subir une sorte de désintégration nucléaire au fil du temps pour devenir stables.[3] Le résultat est une émission d'une certaine forme d'énergie qui se déplace sous forme de « rayon », c'est pourquoi nous l'appelons rayonnement. Comme la demi-vie est une mesure du temps, elle constitue une valeur qui détermine mesurer combien de temps il faudra pour que cette énergie atteigne un état énergétique plus stable.[2]
Différentes substances subissent une perte de leur radioactivité plus rapidement que d'autres. Pour certains éléments radioactifs, la moitié de leurs noyaux instables se désintègrent en moins d'une seconde. Par exemple, le krypton 101 a une demi-vie d'environ dix millionièmes de seconde.[4] En revanche, certains éléments ont une demi-vie extrêmement longue et nécessitent des milliards d'années pour se désintégrer. L'uranium 238 a une demi-vie de 4,51 milliards d'années.[2] Cela signifie qu'il faudrait des milliards d'années pour que l'uranium 238 se désintègre en un rapport de moitié uranium 238 et moitié thorium 234. L'uranium 235 (un autre isotope naturel de l'uranium) a une demi-vie plus courte que l'uranium 238, soit seulement ~700 millions d'années.[4] [4]
Équation
Il existe une équation fréquemment utilisée pour déterminer combien d'une certaine substance radioactive reste après un temps donné. Cela est déterminé à partir de propriétés, telles que la demi-vie d'une substance et la quantité de cette substance présente au départ. L'équation utilisée est la suivante :
où :
- [math]\displaystyle{ N }[/math] est la quantité de la substance après un certain temps
- [math]\displaystyle{ N_o }[/math] est la quantité initiale de la substance
- [math]\displaystyle{ t }[/math] est le temps qui s'est écoulé
- [math]\displaystyle{ t_{1/2} }[/math] est la demi-vie de la substance
Une équation similaire peut être utilisée pour montrer comment l'activité de la substance diminue avec le temps. Pour exprimer cela, l'équation prend la forme :
où :
- [math]\displaystyle{ A }[/math] est l'activité de la substance après un certain temps
- [math]\displaystyle{ A_o }[/math] est l'activité initiale de la substance
- [math]\displaystyle{ t }[/math] est le temps qui s'est écoulé
- [math]\displaystyle{ t_{1/2} }[/math] est la demi-vie de la substance
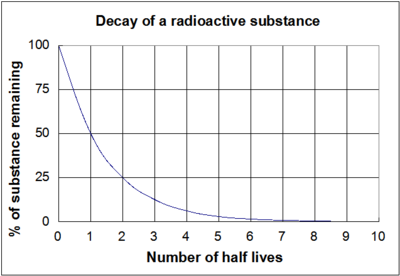
Le graphique de la figure 1 est une représentation visuelle des équations ci-dessus. Il est important de noter que quelle que soit la longueur de la demi-vie (qu'elle soit de plusieurs millions d'années ou de quelques nanosecondes), la forme du graphique sera la même. La connaissance des demi-vies aide les géologues à dater les roches, en utilisant la datation radio-isotopique.
En savoir plus
- Radioactif
- Radioactif vs irradié
- Désintégration radioactive
- Deuxième loi de la thermodynamique
- Ou explorez une page au hasard
Références
- ↑ Created internally by a member of the Energy Education team
- ↑ 2,0 2,1 et 2,2 GCSE Physics. (July 23, 2015). Half Life [Online]. Available: http://www.gcsescience.com/prad16-half-life.htm
- ↑ HyperPhysics. (July 23, 2015). Radioactive Half-Life [Online]. Available; http://hyperphysics.phy-astr.gsu.edu/hbase/nuclear/halfli.html
- ↑ 4,0 4,1 et 4,2 Chart of the nuclides. (July 24, 2015). Half-Life [Online]. Available; http://www.nndc.bnl.gov/chart/reCenter.jsp?z=92&n=143

