« Dioxyde de carbone » : différence entre les versions
energy_french>Paul.frey |
m (1 version importée) |
(Aucune différence)
| |
Version du 13 août 2021 à 06:59
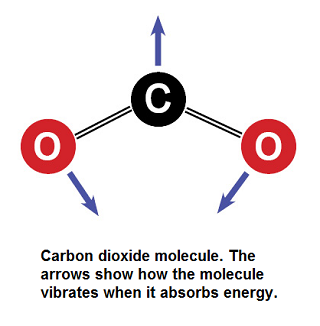
Le dioxyde de carbone (CO2) est un gaz naturel, essentiel au cycle du carbone et un sous-produit de nombreuses formes de production d'énergie. Il s'agit également d'un gaz à effet de serre.
| Formule chimique | CO2 |
| Masse molaire | 44.01 grammes/mole |
Le dioxyde de carbone (voir figure 1) est extrait de l'atmosphère par la photosynthèse dans les plantes pour produire de l'énergie, et par l'absorption chimique de l'océan (ce qui entraîne une acidification des océans). La quantité totale de dioxyde de carbone dans l'atmosphère a toujours été en équilibre avec la respiration des animaux et des plantes. Récemment, une augmentation nette considérable des niveaux de CO2 atmosphérique et océanique a toutefois été observée. Cela est principalement dû au fait que les humains extraient le carbone (sous forme de combustibles fossiles) du sol et le libère dans l'atmosphère. Ces combustibles subissent une combustion, qui produit du dioxyde de carbone comme sous-produit. Chimiquement, le dioxyde de carbone est l'un des deux produits principaux de toute forme de combustion (l'autre étant l'eau).
Potentiel de réchauffement global
Le potentiel de réchauffement global (PRG) est une mesure de la quantité de chaleur qu'un gaz à effet de serre retient dans l'atmosphère. Le CO2 est utilisé comme référence pour cette échelle, le dioxyde de carbone a donc un PRG de 1. La question de savoir combien de temps le dioxyde de carbone reste dans l'atmosphère après son émission est difficile à calculer.[3]
Le dioxyde de carbone laisse passer la lumière visible, mais sa capacité à vibrer sur une échelle moléculaire fait que le CO2 absorbe le rayonnement infrarouge. Ce rayonnement infrarouge est à l'origine de l'augmentation des températures. Veuillez consulter les figures 1 et 2 pour voir comment la molécule vibre pour absorber et réémettre le rayonnement infrarouge.
Émissions
Le carbone est le mot à la mode en matière d'émissions, c'est pourquoi il est important de connaître la différence entre carbone et dioxyde de carbone. Le carbone est un élément présent dans toutes les matières organiques et n'est pas, en soi, un mauvais élément. En fait, le carbone est nécessaire à toute vie. Le dioxyde de carbone, par contre, est ce que la plupart des gens évoquent lorsqu'ils parlent d'émissions de carbone. C'est un gaz à effet de serre et il contribue au changement climatique car il aide à retenir la chaleur dans notre atmosphère. Actuellement, les niveaux de CO2 dans les océans et l'atmosphère sont en hausse, et cette augmentation peut être attribuée en grande mesure aux activités humaines.[4] Ce phénomène est également appelé émission anthropique de CO2. Les émissions de CO2 sont souvent mesurées en gigatonnes de carbone ou dioxyde de carbone. Pour convertir les gigatonnes de carbone en gigatonnes de dioxyde de carbone, il faut multiplier par 44.01/12.01, soit 3.664. Le graphique interactif ci-dessous montre les mégatonnes (1000 mégatonnes = 1 gigatonne) d'émissions de dioxyde de carbone par pays (ou région selon les préférences personnelles).
Des scientifiques à travers le monde recherchent des moyens de capturer le carbone et de l'enfouir sous terre dans un processus appelé séquestration du dioxyde de carbone. Si des méthodes efficaces sont mises au point, cela permettrait à l'humanité de réduire considérablement les niveaux de CO2 atmosphérique et océanique et d'empêcher ainsi une augmentation dangereuse de la température mondiale.
Graphique interactif
Sélectionnez un type de graphique, et le groupe « compare by », et les données choisies apparaîtront dans la boîte ci-dessous.
En savoir plus
- Gaz
- Combustion d'hydrocarbures
- Gaz à effet de serre
- Effet de serre
- Séquestration du dioxyde de carbone
- Ou explorez une page au hasard
Références
- ↑ Bredenberg, Al. (2015, June. 17). Carbon Dioxide -- How Can One Little Molecule Be Such a Big Troublemaker?. [Online]. Available: http://news.thomasnet.com/IMT/2012/03/06/carbon-dioxide-how-can-one-little-molecule-be-such-a-big-troublemaker/
- ↑ PhET Simulations, Molecules and Light [Online], Available: https://phet.colorado.edu/en/simulation/molecules-and-light
- ↑ IPCC. (2015, June. 17) If Emissions of Greenhouse Gases are Reduced, How Quickly do Their Concentrations in the Atmosphere Decrease?. [Online]. Available:http://www.ipcc.ch/publications_and_data/ar4/wg1/en/faq-10-3.html
- ↑ IPCC. (2015, June. 17). Are the Increases in Atmospheric Carbon Dioxide and Other Greenhouse Gases During the Industrial Era Caused by Human Activities? [Online]. Available:http://www.ipcc.ch/publications_and_data/ar4/wg1/en/faq-7-1.html

