« Octane » : différence entre les versions
m (1 version importée) |
m (1 version importée) |
||
| (Une version intermédiaire par un autre utilisateur non affichée) | |||
| Ligne 1 : | Ligne 1 : | ||
[[Category:Finit]] | [[Category:Finit]] | ||
[[en:Octane]] | |||
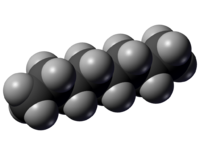
[[File:N-octane-spaceFilling.png|thumb|200px|Figure 1. Modèle de remplissage d'espace de l'éthane. Les sphères grises représentent les atomes d'[[hydrogène]], et les sphères noires - ceux de [[carbone]].<ref>"N-octane-spaceFilling" Licensed under Public Domain via Wikimedia Commons - http://commons.wikimedia.org/wiki/File:N-octane-spaceFilling.png#mediaviewer/File:N-octane-spaceFilling.png</ref>]] | [[File:N-octane-spaceFilling.png|thumb|200px|Figure 1. Modèle de remplissage d'espace de l'éthane. Les sphères grises représentent les atomes d'[[hydrogène]], et les sphères noires - ceux de [[carbone]].<ref>"N-octane-spaceFilling" Licensed under Public Domain via Wikimedia Commons - http://commons.wikimedia.org/wiki/File:N-octane-spaceFilling.png#mediaviewer/File:N-octane-spaceFilling.png</ref>]] | ||
Version actuelle datée du 17 décembre 2021 à 03:43
L'octane est un alcane de formule chimique C8H18. En tant qu'hydrocarbure, l'octane peut être brûlé comme un combustible. À température ambiante, cette molécule organique est un liquide incolore avec une odeur caractéristique d'essence.[2] Son utilisation principale est en tant que composant d'essence, et la performance de cette essence dépend de son indice d'octane, qui tire son nom de cette molécule. Notez, cependant, que le concept de l'indice d'octane est un peu plus compliqué que la simple question de « combien d'octane il y a dans un carburant ». L'équation chimique équilibrée pour la combustion complète de l'octane est :
[math]\ce{ 2C_8H_{18} + 25(O_2)\leftrightarrow 16(CO_2) + 18(H_2O) }[/math]
Propriétés
Voici un tableau de certaines propriétés de base de l'octane:
| Formule chimique | C8H18 |
| Masse molaire | 114.23 grammes/mole |
| Densité énergétique | 47.9 MJ/kg [3] |
| Point de fusion | -57oC[4] |
| Point d'ébullition | 125oC[4] |
Réaction de combustion
Tout comme d'autres hydrocarbures, l'octane subit une combustion d'hydrocarbures en combinaison avec l'oxygène, formant le dioxyde de carbone. L'équation chimique équilibrée pour la combustion complète del'octane est :
La réaction de combustion d'hydrocarbures libère de l'énergie sous forme de chaleur et constitue un exemple de réaction exothermique. La réaction a également une valeur de changement d'enthalpie négative (ΔH).
En savoir plus
- Énergie chimique
- Liaison chimique
- Combustion
- Énergie primaire
- Technologie de conversion d'énergie
- Ou explorez une page au hasard.
Références
- ↑ "N-octane-spaceFilling" Licensed under Public Domain via Wikimedia Commons - http://commons.wikimedia.org/wiki/File:N-octane-spaceFilling.png#mediaviewer/File:N-octane-spaceFilling.png
- ↑ National Center for Biotechnology Information. (2015). Properties of Octane [Online]. Available: http://pubchem.ncbi.nlm.nih.gov/compound/octane#section=Top [February 16, 2015].
- ↑ Glenn Elert. (2015). The Physics Hypertextbook - Chemical Potential Energy [Online]. Available: http://physics.info/energy-chemical/ [February 16, 2015].
- ↑ 4,0 et 4,1 Charles E. Ophardt. (2003). Virtual Chembook - Hydrocarbon Boiling Points [Online]. Available: http://www.elmhurst.edu/~chm/vchembook/501hcboilingpts.html [February 16,2015].