Méthane
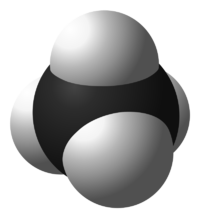
Le méthane est un alcane de formule chimique CH4. En tant qu'hydrocarbure, le méthane est un combustible et dégage de la chaleur lors de sa combustion. Le méthane est le composant principal des hydrocarbures du gaz naturel.[2]
Sous les conditions de températures et de pressions typiques, le méthane est un gaz qui représente environ 95 % de la teneur en gaz naturel liquéfié et environ 80 à 90 % du gaz naturel.[3] Le méthane est aussi un gaz à effet de serre, comme le dioxyde de carbone (CO2). Il a une durée de vie atmosphérique de 12 ans[4], plus brève que celle du (CO2). Cependant, le méthane piège la chaleur plus efficacement que le (CO2), car il possède un (potentiel de réchauffement global) (PRG) de 21[5]
La combustion du méthane (voir la simulation en bas de cette page) fournit une fraction considérable de l'énergie primaire du monde. Elle est utilisée pour le chauffage domestique, la cuisson d'aliments, le chauffage de l'eau et la production d'électricité. Elle peut même fournir de l'énergie pour le transport. Cependant, cela signifie également que le méthane contribue considérablement au changement climatique, car il produit une grande quantité d'émissions de dioxyde de carbone que les humains émettent dans l'atmosphère.
Propriétés
| Formule chimique | CH4 |
| Masse molaire | 16.04 grammes/mole |
| Densité énergétique[6] | 55.5 MJ/kg |
| Point de fusion | -183oC[7] |
| Point d'ébullition | -164oC[7] |
| PRG | 21 |
| Durée de vie atmosphérique | 12 ans |
Animation présentant la combustion
Le méthane libère de l'énergie chimique en subissant une réaction de combustion. Voici une animation de combustion d'hydrocarbures qui montre la réaction globale qui se produit lorsque le méthane se combine avec l'oxygène.
La réaction de combustion d'hydrocarbure libère de l'énergie thermique et constitue un exemple de réaction exothermique. La variation d'enthalpie (ΔH) de cette réaction est donc négative.
Références
- ↑ (2014, Dec. 12). Methane-3D-space-filling [Online]. Available: http://commons.wikimedia.org/wiki/File:Methane-3D-space-filling.svg#mediaviewer/File:Methane-3D-space-filling.svg
- ↑ “NATURAL GAS FAQs,” Pacific Northern Gas RSS. [Online]. Available: http://www.png.ca/natural-gas-faqs/. [Accessed: 24-May-2017]
- ↑ (2014, Jun. 10). Composition of Natural Gas and LNG [Online]. Available: http://www.beg.utexas.edu/energyecon/lng/LNG_introduction_07.php
- ↑ (2014, Jun. 10). Direct Global Warming Potentials [Online]. Available: http://www.ipcc.ch/publications_and_data/ar4/wg1/en/ch2s2-10-2.html
- ↑ Direct Global Warming Potentials [Online]. Available: http://www.ipcc.ch/publications_and_data/ar4/wg1/en/ch2s2-10-2.html [Accessed: 24-May-2017.
- ↑ (2014, Dec. 12). Chemical Potential Energy [Online]. Available: http://physics.info/energy-chemical/
- ↑ 7,0 et 7,1 (2015, Jan. 29). Boiling Points And Structures Of Hydrocarbons [Online]. Available: http://www.elmhurst.edu/~chm/vchembook/501hcboilingpts.html

