« Nonane » : différence entre les versions
energy_french>Luisa Aucun résumé des modifications |
m (1 version importée) |
(Aucune différence)
| |
Version actuelle datée du 17 décembre 2021 à 03:43
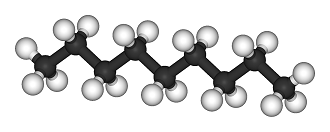
Le nonane est un alcane de formule chimique C9H20. En tant qu'hydrocarbure, il peut subir une combustion et être brûlé comme un combustible. Le nonane est un liquide volatil incolore avec une odeur caractéristique d'essence. Comme d'autres alcanes, le nonane est insoluble dans l'eau.[2]
Normalement, le nonane est obtenu à partir du raffinage du pétrole. Cependant, il peut également être produit en ajoutant de l'hydrogène (H2) au nonène, qui est un alcène apparenté de formule C9H18. Cette réaction s'appelle hydrogénation. Le nonane est également un composant du carburant de l'automobile et du carburéacteur. Le nonane est aussi utilisé comme ingrédient des solvants organiques. Comme le nonane est insoluble dans l'eau, il est donc un bon solvant pour d'autres molécules hydrophobes.[3]
Propriétés
Voici un tableau de certaines propriétés de base du nonane:
| Formule chimique | C9H20 |
| Masse molaire | 128.26 grammes/mole |
| Point de fusion | -51oC[4] |
| Point d'ébullition | 151oC[4] |
Réaction de combustion
Le nonane subit une combustion d'hydrocarbures, se combinant avec l'oxygène pour former le dioxyde de carbone. L'équation chimique équilibrée pour la combustion complète du nonane est :
La réaction de combustion d'hydrocarbures libère de énergie thermique et constitue un exemple de réaction exothermique. La réaction a également une valeur du changement d'enthalpie négative (ΔH).
Références
- ↑ "Nonane-3D-balls". Licensed under Public Domain via Wikimedia Commons - http://commons.wikimedia.org/wiki/File:Nonane-3D-balls.png#mediaviewer/File:Nonane-3D-balls.png
- ↑ National Center for Biotechnology Information. (2015). Properties of Nonane [Online]. http://pubchem.ncbi.nlm.nih.gov/compound/nonane#section=Color [February 16,2015].
- ↑ Andrea Kropp. (2015). Nonane: Structure & Uses [Online]. Available: http://education-portal.com/academy/lesson/nonane-structure-uses.html [February 16, 2015].
- ↑ 4,0 et 4,1 Charles E. Ophardt. (2003). Virtual Chembook - Hydrocarbon Boiling Points [Online]. Available: http://www.elmhurst.edu/~chm/vchembook/501hcboilingpts.html [February 16,2015].